La 16 octombrie 2023, Food and Drug Administration, Agenția Medicamentului din Statele Unite a aprobat tratamentul cu pembrolizumab (Keytruda, Merck), cu chimioterapie care conține platină ca tratament neoadjuvant și cu continuarea pembrolizumabului cu un singur agent ca tratament adjuvant post-chirurgical pentru cancerul pulmonar cu celule mici (NSCLC) rezecabil.
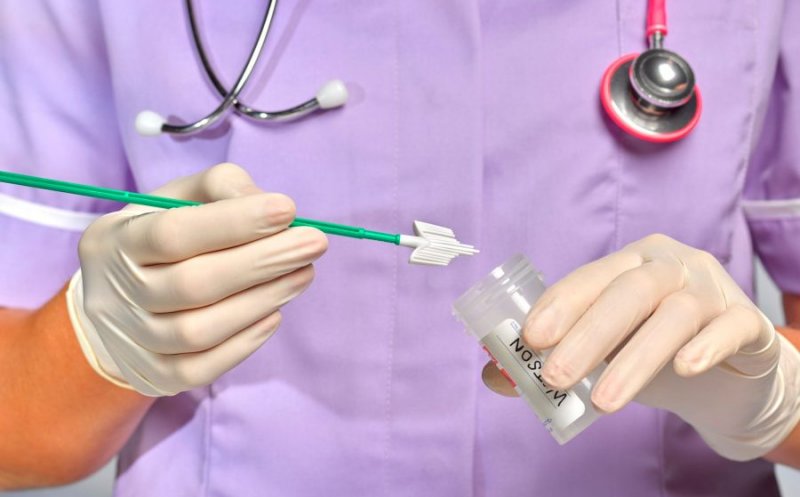
De asemenea, marea noutate este că FDA a aprobat acum ca pacientele nou diagnosticate cu un tip de cancer de col uterin avansat să fie tratate cu Keytruda și în afara studiilor clinice.
Acestea au incluse într-un program de tratament cu imunoterapie, cu acest medicament ani de zile, iar rezultatele au relevat cât este de benefic și în cazul cancerului de col uterin. În prezent, cu Keytruda se tratează 10 tipuri de cancer.
La nivelul României, acest tratament a fost aprbat în centre medicale precum Cluj, Craiova sau București.
Studiu pe 1066 de pacienți
Aprobarea s-a bazat pe date dintr-un studiu clinic efectuat pe 1.060 de paciente pentru care combinaţia de medicamente a redus riscul de progresie a cancerului sau de deces cu 41% în comparaţie cu tratamentul doar cu chimio-radioterapie, a informat firma producătoare Merck.
Tratamentul combinat cu Keytruda a fost aprobat pentru pacientele cu cancer de col uterin care nu au operate și nici incluse pentru tratamentele standard cu radioterapie sau terapie sistemică, a comunicat FDA.
Ajută organismul să lupte împotriva cancerului
Keytruda, ca și alte medicamente folosite în imunoterapie, ajută propriul sistem imunitar al organismului să prevină cancerul prin blocarea unei proteine numite PD-1.
Eficacitatea a fost evaluată în cadrul unuo studiu multicentric, denumit KEYNOTE-671 (NCT03425643).
În cadrul acestuo proiect au fost incluși 797 de pacienți cu NSCLC în stadiul II, IIIA sau IIIB (N2) netratat anterior și rezecabil, în stadiul II, IIIA sau IIIB (N2), conform ediției a 8-a a AJCC.
Pacienții au fost randomizați (1:1) fie la pembrolizumab, fie la placebo, cu chimioterapie pe bază de platină, la fiecare 3 săptămâni, timp de 4 cicluri (tratament neoadjuvant), urmat fie de continuarea tratamentului cu pembrolizumab ca agent unic, fie la placebo, la fiecare 3 săptămâni, timp de până la 13 cicluri (tratament adjuvant).
Detaliile chimioterapiei și fereastra chirurgicală au fost foarte bune, motive pentru care Agenția Națională Americană pentru Alimente și Medicamente a aprobat acest nou tip de tratament împotriva cancerului.
Este foarte cunoscut faptul că FDA aprobă foarte greu noi tratamente împotriva unor boli, și doar după ce sunt efectuate studii de lungă durată, care au concluzii solide care demonstrează eficacitatea noilor medicamente.






Lasă un răspuns